美国国立卫生研究院(NIH)研究人员发现,突变的 RAS 基因可以通过一种新机制促进癌症,从而促进肿瘤生长。这一发现表明,新的联合药物方法可能更有效地治疗由 RAS 引发的癌症。
这一发现可能为 RAS 突变导致的癌症的新型治疗方法铺平道路。
美国国立卫生研究院(NIH)的研究人员及其合作者发现了一种新机制,通过该机制,RAS基因(通常在癌症中发生突变)可以促进肿瘤生长,超越其在细胞表面信号传导中的既定功能。
根据 2024 年 11 月 11 日发表在《自然癌症》杂志上的一项研究,他们发现突变的 RAS 有助于启动一系列涉及特定核蛋白运输的事件,从而导致肿瘤不受控制的生长。
RAS基因是癌症中第二大最常发生突变的基因,而突变的 RAS 蛋白是一些最致命癌症的关键驱动因素,包括几乎所有的胰腺癌、一半的结肠直肠癌和三分之一的肺癌。数十年的研究表明,突变的 RAS 蛋白通过激活细胞表面的特定蛋白质来促进肿瘤的发展和生长,产生持续不断的信号流告诉细胞生长。
理解 RAS 功能的突破
“这是首次有研究显示突变的RAS基因可以以全新的方式促进癌症的发生,”研究作者、美国国立卫生研究院国家癌症研究所 (NCI) 副主任、医学博士 Douglas Lowy 说道:“发现 RAS 蛋白的额外作用对于改善治疗具有令人兴奋的意义。”
阻断突变 RAS 蛋白的药物作为癌症治疗药物问世仅数年,并已获得美国食品药品管理局 (FDA) 批准用于治疗肺癌和肉瘤。尽管 RAS 抑制剂的研发是一项重大的科学成就,但迄今为止,该药物对患者预后的影响有限,仅能使大多数人的生存期延长几个月。
机制:突变RAS如何干扰肿瘤抑制
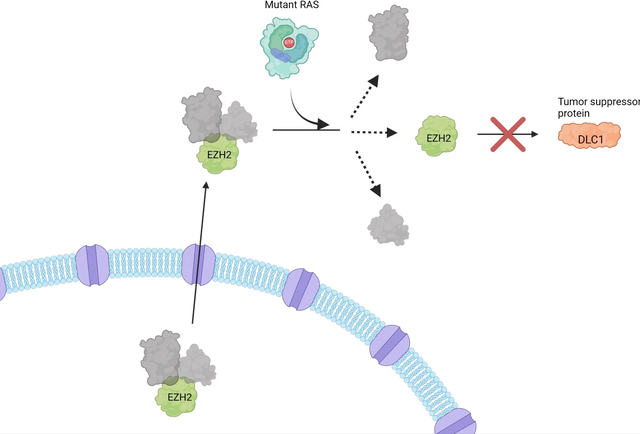
35 年前,Lowy 博士领导的一个研究小组为早期研究做出了贡献,这些研究将RAS确定为致癌基因,并帮助解释了它如何促进肿瘤生长。在这项新研究中,研究小组发现突变的 RAS 直接参与了从细胞核运输到细胞质的复合物中释放一种名为 EZH2 的核蛋白的过程。一旦释放,EZH2 就会促进一种名为 DLC1 的肿瘤抑制蛋白的分解。阻断突变的 RAS 会阻止 EZH2 的释放,从而恢复 DLC1 的活性。
在人类肺癌细胞系和肺癌小鼠模型的实验中,研究人员发现,将 RAS 抑制剂与重新激活 DLC1 肿瘤抑制活性的不同靶向抗癌药物相结合,具有强大的抗癌活性——比单独使用 RAS 抑制剂更有效。
研究还发现证据表明突变的 RAS 蛋白在其他癌症类型中发挥相同的功能,这表明这种机制可能是RAS基因突变癌症的普遍特征。
研究人员认为,他们的研究结果可能对治疗 RAS 引发的癌症具有潜在应用价值。他们已经开始研究 RAS 在胰腺癌中的作用,因为这种类型的癌症的有效治疗方法非常少。
“未来可能会开发出新的治疗组合,将 RAS 的这一新作用考虑在内。”Lowy 博士表示。
参考文献:“RAS•GTP:RanGAP1 复合物的促癌非典型活性促进核蛋白输出”,作者:Brajendra K. Tripathi、Nicole H. Hirsh、Xiaolan Qian、Marian E. Durkin、Dunrui Wang、Alex G. Papageorge、Ross Lake、Yvonne A. Evrard、Adam I. Marcus、Suresh S. Ramalingam、Mary Dasso、Karen H. Vousden、James H. Doroshow、Kylie J. Walters 和 Douglas R. Lowy,2024 年 11 月 11 日,《自然癌症》。DOI:10.1038/s43018-024-00847-5
